 El
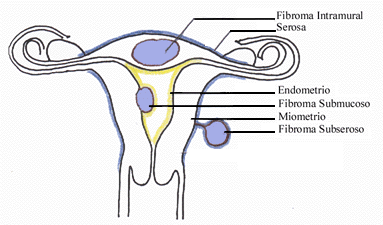
útero humano es un órgano en forma de pera integrado por dos regiones
anatómicas distintas: el cervix y el cuerpo. El cuerpo se divide
adicionalmente en un segmento uterino inferior y en el fundus. El cervix
es un pasaje cilíndrico estrecho que se conecta en su extremo más
inferior con la vagina. En su extremo superior, el cervix se ensancha
para formar el segmento uterino inferior (el isthmo); el segmento
uterino inferior se ensancha en el llamado fondo uterino. El corpus es
el cuerpo del útero que crece durante embarazo para llevar el feto. Las
trompas de falopio (oviductos) se extienden en la parte superior del
utero a cada lado del mismo; estos tubos son continuos con la cavidad
uterina y permiten el pasaje de un óvulo (huevo) de los ovarios al útero
donde el huevo puede implantarse si está fertilizado. El
útero humano es un órgano en forma de pera integrado por dos regiones
anatómicas distintas: el cervix y el cuerpo. El cuerpo se divide
adicionalmente en un segmento uterino inferior y en el fundus. El cervix
es un pasaje cilíndrico estrecho que se conecta en su extremo más
inferior con la vagina. En su extremo superior, el cervix se ensancha
para formar el segmento uterino inferior (el isthmo); el segmento
uterino inferior se ensancha en el llamado fondo uterino. El corpus es
el cuerpo del útero que crece durante embarazo para llevar el feto. Las
trompas de falopio (oviductos) se extienden en la parte superior del
utero a cada lado del mismo; estos tubos son continuos con la cavidad
uterina y permiten el pasaje de un óvulo (huevo) de los ovarios al útero
donde el huevo puede implantarse si está fertilizado.
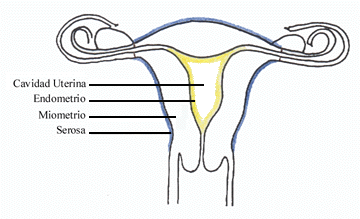 La pared gruesa del útero
esta formada de tres capas: endometrio, miometrio, y serosa. El
endometrio (mucosa uterina) es la capa más interna que cubre
internamente la cavidad del utero. A través del ciclo menstrual, el
endometrio crece progresivamente haciendose más grueso con una fuente
rica de irrigación sanguínea para preparar el útero para la implante
potencial de un embrión. Si no hay implante, una porción de esta capa
es eliminada durante la menstruación. El miometrio es la capa media y más
gruesa del útero y está compuesto de músculo liso (involuntario). El
miometrio se contrae durante la menstruación para ayudar a expeler la
capa endometrial desprendida y durante el parto para propulsar el feto
del útero. La capa exterior, o la serosa, es una capa fibrosa fina,
contigua con las estructuras extrauterinas del tejido conectivo tales
como ligamentos que dan soporte mecánico al útero dentro de la cavidad
pélvica. La pared gruesa del útero
esta formada de tres capas: endometrio, miometrio, y serosa. El
endometrio (mucosa uterina) es la capa más interna que cubre
internamente la cavidad del utero. A través del ciclo menstrual, el
endometrio crece progresivamente haciendose más grueso con una fuente
rica de irrigación sanguínea para preparar el útero para la implante
potencial de un embrión. Si no hay implante, una porción de esta capa
es eliminada durante la menstruación. El miometrio es la capa media y más
gruesa del útero y está compuesto de músculo liso (involuntario). El
miometrio se contrae durante la menstruación para ayudar a expeler la
capa endometrial desprendida y durante el parto para propulsar el feto
del útero. La capa exterior, o la serosa, es una capa fibrosa fina,
contigua con las estructuras extrauterinas del tejido conectivo tales
como ligamentos que dan soporte mecánico al útero dentro de la cavidad
pélvica.
El tamaño uterino de una
mujer no embarazada varía con edad y el número de embarazos, pero mide
aproximadamente tres pulgadas y media de largo y pesa cerca de un
sexto de libra.
References:
-
Cotran, RS, Kumar, V,
and Robbins, SL. Robbins Pathologic Basis of Disease, Fifth Edition.
W.B. Saunders Company, 1994.
-
Netter, FH. Atlas of
Human Anatomy, Sixth Edition. CIBA-GEIGY Corporation, 1993.
Subir al inicio de página
|
Los leiomiomas uterinos,
conocidos comúnmente como fibromas, son tumores no-cancerosos bien
circunscritos, que se presentan en el miometrio (capa de músculo liso)
del útero. Además del músculo liso, los leiomiomas también se
componen de la matriz extracelular (es decir, colágeno, proteoglican,
fibronectina). Otros nombres para estos tumores incluyen fibromiomas,
fibromas, miofibromas, y miomas.
El leiomioma es el tumor pélvico
sólido más común de las mujeres, causando síntomas en
aproximadamente el 25% de las mujeres en edad reproductiva. Pero un exámen
patologico cuidadoso del útero revela leiomiomas en más del 80% porque
los leiomiomas pueden estar presentes pero no son sintomáticos en
muchas mujeres. El útero afectado en promedio tiene seis a siete
fibromas.
Los leiomiomas se detectan
en las mujeres en sus 30 y 40 años y se reducen de tamaño
generalmente después de menopausia en ausencia de terapia de
reemplazo de estrógenos en la post-menopausia. Son dos a cinco veces más
frecuentes en las mujeres negras que en las mujeres blancas. El riesgo
de desarrollar leiomiomas es también más alto en mujeres que son
pesadas para su altura y es más bajo en mujeres que son fumadores y en
mujeres que han dado a luz. Aunque el nivel alto de estrógeno en las píldoras
anticonceptivas orales ha conducido a algunos médicos a aconsejar a
mujeres con leiomiomas evitar usarlos, hay buena evidencia epidemiológica
de que el uso anticonceptivo oral disminuye el riesgo de leiomiomas.
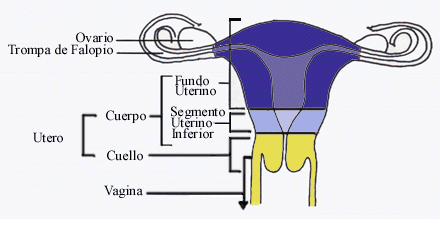 Los
leiomiomas se clasifican por su localización en el útero. Los
leiomiomas subserosos están situados debajo de la serosa uterina y
pueden ser pedunculados (adosados al cuerpo del utero por un tallo
estrecho) o sésiles (de base ancha). Los leiomiomas intramurales se
encuentran predominantemente dentro del grosor del miometrio pero pueden
distorcionar la cavidad uterina o causar un contorno uterino externo
irregular. Los leiomiomas submucosos están situados debajo de la mucosa
uterina (endometrio) y, como los leiomiomas subserosos, pueden ser tanto
pedunculados o sésiles. La mayoría (95%) de todos los leiomiomas
tienen localizaciones subserosas o intramurales; los leiomiomas
submucosos constituyen el 5% restante. Los
leiomiomas se clasifican por su localización en el útero. Los
leiomiomas subserosos están situados debajo de la serosa uterina y
pueden ser pedunculados (adosados al cuerpo del utero por un tallo
estrecho) o sésiles (de base ancha). Los leiomiomas intramurales se
encuentran predominantemente dentro del grosor del miometrio pero pueden
distorcionar la cavidad uterina o causar un contorno uterino externo
irregular. Los leiomiomas submucosos están situados debajo de la mucosa
uterina (endometrio) y, como los leiomiomas subserosos, pueden ser tanto
pedunculados o sésiles. La mayoría (95%) de todos los leiomiomas
tienen localizaciones subserosas o intramurales; los leiomiomas
submucosos constituyen el 5% restante.
Aunque los médicos utilizan
extensamente este esquema de clasificación, tiene la limitación de que
son pocos los leiomiomas que son realmente de tipo "puro." La
mayoría de los leiomiomas tienen más de una localización anatómica
y, por lo tanto, son híbridos (por ejemplo, un leiomioma
predominantemente intramural con un componente submucoso). Otros tipos
de leiomiomas incluyen los miomas "parasitos," que reciben su
fuente de sangre de estructuras diferentes del útero (por ejemplo, el
epiplón), y los miomas tipo semilla, que tienen un diámetro inferior o
igual a cuatro milímetros.
La transformación de los
leiomiomas uterinos (benignos) en leiomiosarcomas uterinos (tumores
malignos del músculo liso del útero) es extremadamente inusual, y, de
hecho, muchos investigadores y clínicos creen que nunca ocurre este
tipo de transformación. Sin embargo, sin la examinación patológica
del útero, no es posible determinar si es el caso. Los leiomiosarcomas
uterinos se encuentran en aproximadamente el 0.1% de las mujeres con
leiomiomas y se ha reportado que están frecuentemente asociados con
fibromas grandes o que crecen rápidamente. Por lo tanto, en mujeres con
estos tipos de tumores se puede considerar una intervención quirúrgica
para descartar el leiomiosarcoma, una lesión poco común pero médicamente
importante.
Subir al inicio de página
|
Investigación indica que
entre el 20% y el 50% de las mujeres tiene síntomas relacionados a
fibromas. Los dos síntomas más comunes de los fibromas (también
llamados leiomiomas) son sangrado uterino anormal y opresión pélvica.
La anormalidad más común
de sangrado es menorragia (sangrado uterino prolongado y/o profuso,
también llamado hipermenorrea). Los períodos menstruales normales
duran típicamente cuatro a cinco días, mientras que las mujeres con
fibromas tienen a menudo períodos que duran más de siete días. Las
mujeres con fibromas también pueden tener sangrado profuso, pueden
necesitar cambiarse las toallas sanitarias con más frecuencia (quizás
cada hora) o dudar en realizar sus actividades normales por el miedo a
una situación embarazosa por el sangrado que presentan. El sangrado
entre los períodos usualmente no se asocia a los fibromas y debe ser
siempre investigado por un médico. Aunque el sangrado anormal puede
ocurrir con cualquiera de las tres clases de fibromas, las mujeres con
los fibromas submucosos parecen particularmente propensas a esta
complicación.
La sensación de presión pélvica
es resultado de un aumento en el tamaño del útero o de un fibroma en
particular. La mayoría de las mujeres con leiomiomas tienen un útero
agrandado; de hecho, los médicos describen el tamaño de un útero
confibromas como un útero de una mujer embarazada, por ejemplo, un útero
con fibromas como uno de 12 semanas de embarazo. No es inusual para un útero
con leiomiomas alcanzar la talla de un utero con embarazo de cuatro a
cinco meses. Además de sensaciones vagas de presión porque un útero
fibromatoso generalmente tiene una forma irregular (teniendo muchas
zonas sobresalientes), las mujeres pueden experimentar una sensación de
presión en las estructuras pélvicas adyacentes incluyendo el intestino
y/o la vejiga. La presión en estas estructuras puede dificultar los
movimientos del intestino y producir estreñimiento o frecuencia e
incontinencia urinaria. Inusualmente, los fibromas pueden presionar los
uréteres (que llevan la orina de los riñones a la vejiga) pudiendo
conducir a disfunción renal.
Los leiomiomas también se
asocian a un espectro de disfunción reproductiva incluyendo aborto
recurrente, infertilidad, trabajo de parto prematuro, malpresentationes
fetales, y complicaciones del trabajo de parto. Aunque existen pocos
estudios sobre la disfunción reproductiva vinculada a los fibromas, la
perspectiva clínica que prevalece es que estas complicaciones se
presentan más a menudo cuando los fibromas se tuercen físicamente
en la cavidad uterina. Por lo tanto, las mujeres con fibromas grandes o
sintomáticos pueden elegir realizarse una evaluación de la cavidad
uterina (por ejemplo por histerosalpingografía o por histeroscopía,
ver abajo), antes de intentar embarazarse. Si los fibromas que se
detectan en el interior del útero (llamados fibromas submucosos), se
tuercen, distorsionando la mucosa uterina, son una causa significativa
de problemas reproductivos y deben ser extirpados. Es menos claro si los
fibromas en la pared del útero causan problemas reproductivos.
Generalmente, si el útero es pequeño, los fibromas no necesitan ser
extirpados en mujeres que comtemplan o desean embarazarse.
El diagnóstico de los
leiomiomas generalmente es determinado fácilmente por la examinación pélvica
bimanual. Durante este examen rutinario, el médico evalúa el tamaño y
la forma del útero y de las estructuras pélvicas que lo rodean
introduciendo dos dedos de una mano en la vagina mientras palpa el
abdomen del paciente sobre el hueso del pubis con la otra mano. Durante
este examen, un útero con fibromas se siente agrandado e irregular y a
menudo puede sentirse en el abdomen por encima del hueso del pubis. En
contraste, un útero sin embarazo y sin fibromas no es palpable por
encima del hueso del pubis.
Además, los estudios de
imagen como por ejemplo la ultrasonografía, MRI (imágenes de la
resonancia magnética), y CT (tomografía computarizada) pueden ser útiles
en confirmar el diagnóstico. Actualmente, la ultrasonografía es el método
más común para confirmar el diagnóstico de leiomiomas, pero MRI puede
ser el método más útil porque puede distinguir a menudo leiomiomas de
otras lesiones intramurales.
En los pacientes que
experimentan menorragia (flujo menstrual profuso y/o prolongado) o pérdidas
recurrentes en su embarazo, la evaluación de la cavidad uterina es
importante porque la presencia de un fibroma submucoso puede escapar a
un ultrasonido tradicional. Hysterosalpingografía, sonohisterografía,
y lahisteroscopía pueden proveer esta información y le ayudaran a un
diagnóstico más definitivo de los fibromas. Procedimientos más
invasivos tales como laparoscopía pueden también ayudar a alcanzar un
diagnóstico definitivo.
La histerosalpingografia y
la sonohisterografía utilizan Rayos X y ultrasonido, respectivamente,
para visualizar la cavidad uterina después de que un tinte específico
se inyecta en el útero. La histeroscopía permite la visualización
directa de la cavidad uterina al introducir una cámara fotográfica
pequeña en el extremo de un tubo largo (hysteroscopio) directamente en
el útero a través de la vagina y del cervix. La laparoscopía, por
otra parte, permite la visualización directa del exterior del útero y
de las estructuras pélvicas circundantes introduciendo una cámara
fotográfica pequeña en el extremo de un tubo (laparoscopio)
directamente en la cavidad abdominal.
Subir al inicio de página
|
En general, los fibromas
solamente necesitan ser tratados si están causando síntomas. El
tratamiento primario para los pacientes con fibromas grandes o
sintomáticos es la cirugía. La histerectomía (retiro quirúrgico del
útero) es la técnica operativa más frecuentemente usada para tratar
este problema. Los fibromas son responsables de aproximadamente un
tercio de histerectomías (o cerca de 200,000 procedimientos) anualmente
en los Estados Unidos.
Hay diferentes tipos de
histerectomías incluyendo histerectomía abdominal, histerectomía
vaginal, histerectomía supracervical, e histerectomía vaginal asistida
laparoscopicamente. El tipo de histerectomía elegido depende del tamaño
del útero, del historial médico de la mujer, y de las habilidades de
su cirujano. La ventaja de la histerectomía en el tratamiento de
leiomiomas es que proporciona a una " curación verdadera "
para los fibromas, pero es solamente una opción para las mujeres que no
planean embarazos futuros.
Cuando las mujeres desean
preservar su capacidad reproductiva, se puede realizar una
miomectomía. A diferencia de la histerectomía en la cual se quita el
útero entero, la miomectomía es un procedimiento quirúrgico en el
cual se quita el fibroma (o fibromas) individualmente. Aproximadamente
18,000 miomectomías se realizan anualmente en los Estados Unidos. La
mayoría de las miomectomías se realizan a través de una incisión
abdominal, aunque ciertos fibromas submucosos se pueden retirar a través
de la vagina sin una incisión abdominal durante un procedimiento
llamado miomectomía histeroscopica en el cual se utiliza un instrumento
especial llamado histeroscopio. Esta técnica es sobre todo útil para
las mujeres con sangrado o problemas relacionados al embarazo pues hay
generalmente pequeños cambios en el tamaño del útero con esta técnica.
Ciertos fibromas subserosos se pueden retirar abdominalmente durante un
procedimiento llamado miomectomia laparoscopica en el que se utiliza un
instrumento diferente llamado laparoscopio. En el general,
la miomectomía disminuye la menorragia (flujo menstrual profuso y/o
prolongado ) en el 80% de los pacientes que se presentan con este síntoma.
Desafortunadamente, hay un riesgo significativo de recurrencia de
fibromas después de una miomectomía; en algunos estudios hasta un 10%
de las mujeres que experimentaron un miomectomía inicial requeriran un
segundo procedimiento operativo. Además, de un cuarto a la mitad de las
mujeres que experimentaron miomectomías tuvieron evidencia por
ultrasonido de la recurrencia de sus fibromas en el plazo de uno a diez
años.
Hay también varias técnicas
innovadoras que estan siendo estudiadas como posibles tratamientos quirúrgicos
para el sangrado relacionado a los fibromas. La Miolisis involucra
transmitir corriente eléctrica a través de agujas a un fibroma en el
momento de la laparoscopía . La Criomiolisis involucra el uso de una
punta que congela con resultados similares. La embolization de la
arteria uterina es un alternativa radiológica a la cirugía que
involucra la colocación de un catéter en una arteria en la pierna y
dirigir el catéter utilizando imágenes radiográficas a las arterias
del útero. Una vez allí, el catéter se utiliza para administrar
agentes que bloquean estos vasos sanguíneos importantes. Mientras que
todos estos tratamientos pueden ser eficaces para los fibromas,
comparados a las opciones más tradicionales, el número de los
pacientes tratados por estos métodos ha sido pequeño, el seguimiento
relativamente de corto plazo, y no se ha demostrado que estos
procedimientos son seguros en mujeres que desean quedar embarazadas.
Subir al inicio de página
|
Ciertas medicinas pueden
ayudar a controlar los síntomas relacionados a los fibromas. Los
medicamentos más eficaces para el tratamiento de fibromas son los
agonistas de la Hormona Liberadora de gonadotropina(GnRH) (incluyendo
Lupron, Synarel, Zoladex). Los agonistas de GnRH inducen un estado de
estrógeno-bajo (parecido al de la menopausia). Debido a que los
fibromas son dependientes del estrógeno para su desarrollo y
crecimiento, la inducción de un estado bajo de estrógeno causa la
reducción de la masa del tumor y del útero, aliviando los síntomas de
la presión ejercida por estos (específicamente, se ha demostrado que
el volumen uterino disminuye aproximadamente en 50% después de tres
meses de la terapia agonista de GnRH.) Además de disminuir el tamaño
del útero, el tratamiento con los agonistas de GnRH también detiene el
flujo menstrual (amenorrea), permitiendo que las mujeres con anemia
inducida por el sangrado, tengan aumentos visibles en sus dépositos de
hierro. Desafortunadamente, la interrupción del tratamiento con el
agonista de GnRH es seguida por un nuevo crecimiento rápido de los
fibromas y del útero al volumen del pre-tratamiento. Además, debido a
que el hueso también requiere de estrógeno, el uso a largo plazo de
los agonistas de GnRH puede disminuir perceptiblemente la densidad del
hueso y puede conducir a pérdida ósea u osteoporosis. Actualmente, por
lo tanto, el uso de los agonistas de GnRH se limita generalmente a un
curso preoperativo corto de uno a tres meses para contraer el útero y
facilitar un procedimiento quirúrgico o para inducir a una amenorrea
que mejore la condición hematológica antes de cirugía.
La combinación de los
agonistas de GnRH y las dosis bajas de las hormonas esteroideas
estrógeno y progesterona (es decir, los regímenes de "reemplazo
") se ha empleado en algunos ensayos clínicos en un intento por
prolongar con seguridad la duración máxima de la terapia con los
agonistas de GnRH sin sacrificar su eficacia. Estos regímenes se han
estudiado para su uso de hasta dos años. Datos preliminares sugieren
que éstos pueden ser seguros y eficaces si la dosis de la hormona es
baja (equivalente a las dosis de reemplazo en la menopausia contra píldoras
para el control de la natalidad en dosis altas) y si el agonista de la
GnRH se da primero, permitiendo que el útero se contraiga antes de que
se administren las hormonas. Este acercamiento parece mantener la
reducción del utero y/o controlar el sangrado uterino mientras que
ayuda a mantener otros tejidos tales como el hueso y reducir al mínimo
los efectos secundarios tales como bochornos que acompañan a los
niveles bajos de estrógeno inducidos por la terapia de los agonistas de
la GnRH.
Varias opciones innovadoras
están bajo investigación como posibles tratamientos médicos futuros
para los leiomiomas uterinos. Varios estudios pequeños han analizado el
uso de los antagonistas de GnRH en leiomiomas. La ventaja principal de
los antagonistas sobre los agonistas de la GnRH más extensamente usados
es que los antagonistas comienzan a actuar más rápidamente. Sin
embargo para la terapia a largo plazo, los antagonistas parecen no tener
ninguna ventaja.El antagonista de la progesterona ,el mifepristone (RU
486), también ha demostrado en estudios pequeños inducir la reducción
uterina y detener la menstruación en mujeres con fibromas. Estudios del
medicamento antifibrótico, pirfenidone, están también en el proceso
de determinar si este agente es útil en el tratamiento de los fibromas.
Otras terapias médicas
incluyendo los agentes androgénicos (por ejemplo, danazol, gestrinone),
las progestinas (por ejemplo, acetato del medroxiprogesterona, acetato
de depomedroxiprogesterona, noretindrone), y las píldoras
anticonceptivas orales también han sido utilizadas para controlar la
menorragia (flujo menstrual prolongado y/o profuso) en mujeres con
leiomiomas, probablemente disminuyendo el endometrio (atrofia
endometrial). Sin embargo, estos medicamentos no reducen
consistentemente el tamaño del útero o el volumen del fibroma y son a
menudo ineficaces para controlar la menorragia.
Subir al inicio de página
|
A pesar del impacto
importante de los leiomiomas en salud pública, poco se sabe sobre la
causa que los origina. Hasta hace poco tiempo, las hormonas esteroideas,
el estrógeno y progesterona, eran consideradas las reguladoras más
importantes del crecimiento del leiomioma. Hay evidencia abundante de
que el estrógeno promueve el crecimiento del fibroma, incluyendo
observaciones clínicas que muestran que los fibromas crecen en
presencia de altos niveles de estrógeno, por ejemplo durante los años
reproductivos, y que su tamaño se reduce en presencia de niveles bajos
de estrógeno, tal como ocurre después de la menopausia o durante la
terapia con mujeres que fueron tratadas con la hormona liberadora de
gonadotropina (GnRH). Además, los fibromas tienen altas concentraciones
de estrógeno, tienen más receptores de estrógeno, y convierten el
estradiol (una forma más activa de estrógeno) a estrona (una forma
menos activa de estrógeno) más lentamente que el miometrio normal.
La progesterona también se
piensa que desempeña un rol en el crecimiento del fibroma. Más específicamente,
los estudios clínicos sugieren que la progesterona facilita el
crecimiento de fibromas. Por ejemplo, el tamaño del fibroma aumenta
durante el tratamiento con progesteronas sintéticas. La terapia
combinada del agonista de la GnRH y de la progesterona ha
demostrado no tener ningún efecto en el volumen uterino, en contraste a
la terapia del agonista de GnRH la cual ha demostrado reducir el
volumen uterino. La observación de que los fibromas regresionan con el
agente antiprogesterona, RU-486, apoya el papel de la progesterona como
promotor del crecimiento del fibroma. Histológicamente, los fibromas de
los pacientes tratados con progesterona muestran más crecimiento
celular que aquellos de pacientes sin terapia con progesterona. Bioquímicamente
los fibromas tienen concentraciones más altas del receptor de la
progesterona que las del miometrio normal. Juntos, estos datos sugieren
que la progesterona también incrementa el crecimiento del fibroma.
Otras hormonas tales como la
hormona del crecimiento (GH) y la prolactina (PRL) también se piensan
que promueven el crecimiento del fibroma, pero su papel está aún menos
definido.
Más recientemente se ha
mostrado que los factores de crecimiento, que son proteínas pequeñas
que afectan el crecimiento célular median los efectos del estrogeno que
promueven el crecimiento y desempeñan un papel importante en el
desarrollo de los fibromas. Los factores potencialmente importantes en
el crecimiento del fibroma incluyen el factor transformante-beta de
crecimiento, factor de crecimiento básico del fibroblasto, factor
de crecimiento epidérmico, factor de crecimiento parecido a la insulina,
y factor de crecimiento derivado de plaquetas.
Todos, el estrógeno, la
progesterona, y los factores del crecimiento promueven probablemente el
crecimiento del tumor, pero solamente después del inicio de la formación
del tumor. Este acontecimiento inicial sigue siendo desconocido,
aunque la evidencia reciente sugiere que hay un fuerte componente
hereditario al desarrollo de los fibromas. La evidencia indirecta para
esta hipótesis es como sigue. Primero, los fibromas son por lo menos
dos veces más comunes en las mujeres negras que en las mujeres blancas.
Aunque las diferencias raciales en status socioeconómico y en acceso al
cuidado médico, así como las diferencias raciales son factores de
riesgo conocidos para los fibromas, pueden contribuir a este hallazgo,
dos estudios recientes sugieren que estos factores no explican en su
totalidad esta discrepancia. En segundo lugar, otro estudio encontró
una predisposición genética para la histerectomía según lo indicado
por una correlación dos veces más alta para la histerectomía en
gemelos idénticos contra gemelos fraternos. En tercer lugar, existe una
forma hereditaria rara de fibromas uterinos en asociación con los
fibromas de la piel llamada el síndrome de Reed's. Finalmente, estudios
recientes en Rusia sugieren que las mujeres con antecedentes familiares
de fibromas son dos veces más propensas a desarrollar fibromas que
mujeres sin antecedentes familiares. Desafortunadamente, pocos estudios
científicos examinan directamente el componente genético del
desarrollo del fibroma.
Recientemente, los
investigadores en el centro para Fibromas Uterinos han identificado
mutaciones en dos genes, HMGI(c) y HMGI(y), que parecen ser importantes
en el desarrollo de algunos fibromas. (Para más información sobre la
genética de fibromas, vea los artículos publicados para estos
genes en la página de " publicaciones ".) Normalmente, estos
genes codifican para las proteínas que ayudan al control del
crecimiento celular indirectamente regulando la transcripción del DNA.
Sin embargo, las mutaciones
en estos genes son probablemente cambios secundarios en células genéticamente
susceptibles. Por lo tanto, es probable que existan otros genes
cruciales para el desarrollo de los fibromas que todavía no se han
identificado. Al respecto, el personal en el Centro de Fibromas Uterinos
está estudiando familias con por lo menos un par de hermanas afectadas
por los fibromas para buscar el gen (o los genes) que predisponen a las
mujeres al desarrollo de fibromas. Para información sobre este estudio,
incluyendo la participación, vea por favor, " Encontrando genes
para los fibromas(Finding genes for fibroids)" en la página de los
" estudios actuales ".
En última instancia,
conocer las hormonas, los factores del crecimiento, y los genes
implicados en la formación y el crecimiento de fibromas pueden conducir
a opciones innovadoras, menos invasoras de tratamiento.
Subir al inicio de página
|
Definición, prevalencia, y causa
La Adenomiosis es una enfermedad benigna del útero en la cual componentes
normalmente limitados al endometrio (la capa interna más delgada del útero) son encontrados
en el miometrio (la capa muscular media del útero). La prevalencia exacta de adenomiosis no
es conocida porque el diagnóstico puede ser hecho sólo por examen microscópico de muestras
uterinas obtenidas durante una cirugía, o menos frequente cuando se efectúa una biopsia de
endometrio por otra causa. Algunos estudios consideran que el 20% de las mujeres tienen
adenomiosis, sin embargo por medio de un análisis microscópico cuidadoso de múltiples
muestras de miometrio de un mismo individuo, incrementa la prevalencia hasta en un 65%.
La causa de adenomiosis es también desconocida. La teoría mas aceptada
acerca del desarrollo de adenomiosis propone que la barrera entre el endometrio y el
miometrio se encuentra alterada, la cual normalmente previene invasión de las glándulas
endometriales y el estroma hacia el miometrio, esta alteración permite que ocurra invasión
hacia el miometrio. Se piensa que este proceso solo ocurre bajo la presencia de estrógenos,
sin embargo, existe muy poca evidencia científica que apoye esta hipótesis.
La adenomiosis es más frecuente entre los 40 y 50 anos, y se asocia con
historia de embarazos previos ya que el 80% de mujeres con esta enfermedad han tenido hijos
antes. Sin embargo, la incidencia de adenomiosis no se correlaciona con el incremento en el
número de embarazos.
La adenomiosis es también asociada con otros trastornos uterinos. Mas del
80% de las mujeres con adenomiosis tienen otro proceso patológico asociado en el útero; 50%
de las pacientes tienen fibromas (tumores benignos del músculo liso del
útero), 11% tienen endometriosis (tejido endometrial afuera del útero, mas común en los
ovarios), y 7% tienen pólipos endometriales (sobrecrecimiento benigno del tejido
endometrial). Los síntomas de estas patologías asociadas a menudo obscurecen el diagnostico
de adenomiosis.
Síntomas y diagnóstico
Un útero típico con adenomiosis es blando y aumentado de tamaño en forma
uniforme. Aproximadamente el 80% de úteros con adenomiosis pesan más de 80 gramos (un útero
normal pesa alrededor de 50 gramos), pero no es inusual que algunos lleguen a pesar más de
200 gramos.
Los síntomas de adenomiosis incluyen sangrado uterino anormal
(aproximadamente en el 60% de las mujeres) y dolor pélvico.
El sangrado uterino anormal se puede manifestar ya sea como hipermenorrea
(sangrado uterino abundante y/o prolongado) o metrorragia (sangrado irregular). Dismenorrea
(dolor pélvico durante la menstruación) es el segundo síntoma más común en pacientes con
adenomiosis, ocurriendo en el 25% de los casos.
Una revisión de la literatura demuestra que solo en el 15% de los casos de
adenomiosis el diagnóstico fué correcto antes de la cirugía. Hay dos motivos por las cuales
el porcentaje de diagnóstico pre-quirúgico es tan pequeño; el primero es que muchas
pacientes con adenomiosis son asintomáticas, y no se encuentra presente otra patología
uterina asociada que haga al médico estudiar ese útero, y el segundo motivo es debido a que
esta enfermedad es a menudo enmascarada por otra patología asociada (ejemplo, leiomiomas,
endometriosis).
Dilatación y curetaje no son de ayuda para efectuar el diagnostico. (En este
procedimiento, el cérvix es dilatado gradualmente para posteriormente remover una porción
pequeña de epitelio uterino dañado y observarlo ante el microscopio que es lo que llamamos
biopsia). La ecografía pélvica puede ser sugestiva pero no es definitiva en proporcionar el
diagnóstico. La utilidad de otros estudios imagenológicos tales como el uso de resonancia
magnética nuclear (RMN) es actualmente indeterminada.
Tratamiento
Las áreas de adenomiosis no se pueden extraer por medio de cirugía local.
Por lo que el único tratamiento definitivo es la histerectomía total (extracción quirúrgica
de todo el útero).
El tratamiento hormonal como el uso de hormonas esteroideas sintéticas como
los progestágenos no son útiles y pueden incrementar el nivel de dolor pélvico en algunas
pacientes. Agonistas de la hormona liberadora de gonadotropinas (GnRH) han sido usados en
algunos casos, resultando en una disminución importante del tamaño uterino, provocan
amenorrea (ausencia de menstruaciones), y también pueden interferir en la fertilidad de la
mujer.
Desafortunadamente, los síntomas de la adenomiosis pueden recurrir ya que
hay un re-crecimiento del tejido anormal y la recurrencia es usualmente documentada en los
primeros 6 meses después de haber suspendido la terapia.
Subir al inicio de página
|

